珠海舒桐医疗科技有限公司
5 年
手机商铺
- NaN
- 0.5999999999999996
- 0.5999999999999996
- 1.5999999999999996
- 0.5999999999999996
珠海舒桐医疗科技有限公司
入驻年限:5 年
- 联系人:
柳嘉欣
- 所在地区:
广东 珠海市 香洲区
- 业务范围:
试剂、技术服务、抗体、细胞库 / 细胞培养、ELISA 试剂盒、耗材、原辅料包材
- 经营模式:
科研机构 生产厂商
推荐产品
公司新闻/正文
Nucleic Acids Research | Cas9的“分子胶水”效应:通过激活核糖体-mTORC2通路调控细胞生长
107 人阅读发布时间:2025-11-19 17:49
Nucleic Acids Research | Cas9的“分子胶水”效应:通过激活核糖体-mTORC2通路调控细胞生长
研究亮点
本研究采用的系统性研究方法具有多个显著优势,使其在基因编辑安全性评估领域具有开创性意义。
1. 广泛的细胞类型覆盖:涵盖32种细胞系(10种癌症类型+非癌细胞),揭示Cas9效应的细胞类型特异性,为理解其作用背景提供关键数据。
2. 多维度机制解析:整合互作组学(Cas9结合蛋白)、转录组学(基因表达变化)和功能验证,从现象到机制层层深入。
3. 发现全新作用机制:首次揭示Cas9作为“分子胶水”,通过增强核糖体蛋白(RPL26/RPL23a)与mTORC2核心亚基Sin1的相互作用,绕过生长因子需求激活mTORC2/Akt通路促进细胞生长。
4. 明确临床相关性:聚焦mTORC2/Akt通路(癌症关键通路),发现Cas9能在血清饥饿(模拟肿瘤微环境)下维持其活性,对基因治疗安全性评估具重要启示。
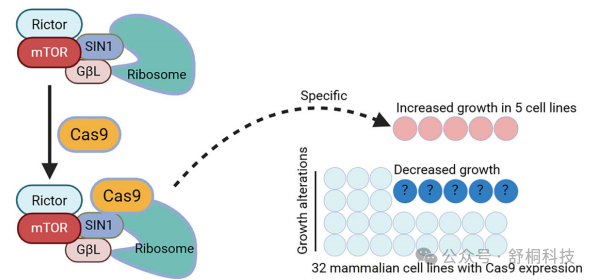
核心技术介绍与研究背景
CRISPR-Cas9基因编辑技术是当今生物医学领域最具革命性的技术之一,其核心在于利用细菌来源的Cas9核酸酶在特定向导RNA的引导下,实现对基因组特定位点的精准切割和编辑。这项技术源自细菌的适应性免疫系统,通过将外源DNA片段整合到CRISPR序列中,形成对特定病原体的记忆性防御。在工程化应用中,研究人员通过将Cas9核酸酶与人工设计的sgRNA共同导入细胞,实现对目标基因的敲除、插入或修饰,为基因功能研究、疾病模型构建和基因治疗开辟了全新途径。
近年来,CRISPR-Cas9技术已在基础研究和临床治疗中展现出巨大潜力。从实验室的基因功能筛选到FDA批准的代表性CRISPR疗法治疗镰状细胞病,该技术的应用范围不断扩大。然而,随着研究的深入,科学家们开始关注这一技术的安全性问题,特别是Cas9作为细菌来源的核酸酶在哺乳动物细胞中长期表达可能产生的非预期效应。
本研究于2025发表在期刊《Nucleic Acids Research》,系统性地探讨了稳定表达SpCas9对哺乳动物细胞生长的影响,并揭示了这些变化背后的分子机制。研究团队通过分析32种细胞系(涵盖10种癌症类型和非癌细胞)发现,Cas9的稳定表达在一部分细胞系中会显著改变细胞生长特性。这一发现不仅对CRISPR技术的安全性提出了重要警示,更揭示了Cas9核酸酶通过调控细胞内信号通路影响细胞行为的新机制。
研究主要解决了三个关键问题:首先,稳定表达Cas9是否普遍影响哺乳动物细胞的生长行为;其次,这种影响背后的分子机制是什么;最后,这些发现对CRISPR技术的进一步应用有何启示。通过对这些问题的深入探究,研究为优化基因编辑工具、提高治疗安全性提供了重要科学依据。
关键实验结果与机制解析
稳定Cas9表达对多种细胞系生长的影响
研究团队首先建立了32种细胞系的Cas9稳定表达模型,通过慢病毒感染将Flag标记的SpCas9导入细胞,并使用相同的病毒骨架但不含Cas9编码序列的载体作为阴性对照。通过Western blot验证了Cas9在各细胞系中的表达情况。为评估细胞生长变化,研究采用了二维集落形成实验,将等量细胞接种后培养7-21天,直至形成可见集落,通过结晶紫染色和手动计数来量化集落形成能力。每个实验均设置了多个生物学重复,并由至少两名独立研究人员进行评估,确保了结果的可靠性。

图1 稳定表达SpCas9对细胞生长影响的表征分析
重要实验结论
1. Cas9表达在不同细胞系中产生差异性生长效应:在阴性对照感染不影响生长的细胞系中,SpCas9表达导致五种细胞系(RCC4、MDA-MB-231、MDA-MB-453、DU145和PC3)生长加快,而在2种细胞系(MCF-7和MIA PaCa-2)中抑制生长,其余细胞系未显示明显变化(图1U)
2. 病毒载体感染本身即可影响部分细胞系的生长:在11种细胞系中,仅阴性对照病毒感染就显著降低了细胞生长,这提示在CRISPR实验设计中需谨慎考虑病毒感染的潜在影响(图1U)
3. Cas9对细胞生长的影响与NRF2稳定性无必然关联:尽管之前研究发现Cas9可通过竞争性结合Keap1稳定NRF2,但本研究显示生长变化与NRF2水平不完全相关,表明存在其他机制主导(图1A-J)
Cas9相互作用组揭示核糖体蛋白为关键结合伙伴
为探究除Keap1抑制之外Cas9表达诱导细胞生长改变的原因,研究团队选择了两株在Cas9表达后显示细胞生长增加的细胞系(DU145和MDA-MB-231)进行蛋白质相互作用组分析。通过Flag免疫共沉淀联合质谱分析,系统鉴定了与Cas9特异性结合的蛋白质。实验使用稳定表达Flag-Cas9或对照的细胞,裂解后与Flag-M2琼脂糖珠孵育,洗脱结合蛋白后通过液相色谱-质谱联用技术进行鉴定。数据分析采用MaxQuant软件,以 Homo Sapiens 数据库为参考,设定结合蛋白的阈值为| log2(fold change)≥1|且P值<0.05。
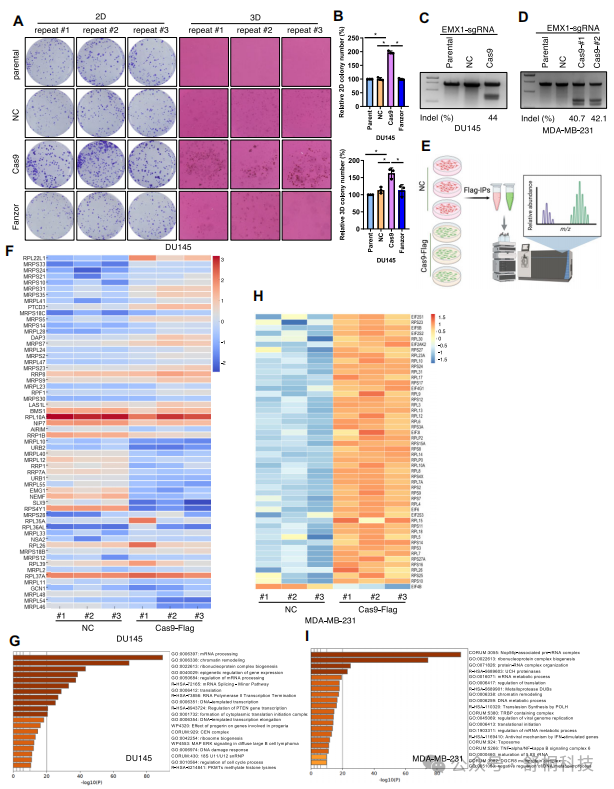
图2 SpCas9相互作用组鉴定核糖体蛋白为关键共享结合因子
重要实验结论
1. 核糖体蛋白是Cas9的主要结合伙伴:在DU145和MDA-MB-231细胞中,核糖体蛋白(包括RPL和RPS家族)均是Cas9相互作用组中最显著的共同成分(图2F-I)
2. Cas9与核糖体的结合具有细胞类型特异性:虽然核糖体蛋白是共同的主要结合伙伴,但不同细胞系中具体的结合蛋白谱存在差异,表明细胞环境影响Cas9的相互作用网络(图2F-H)
3. Cas9保持有效的基因编辑活性:在用于互作组分析的细胞中,T7E1检测证实Cas9仍具有高效的基因组编辑能力,排除了因蛋白功能失常导致效应的可能性(图2C-D)
Cas9通过mTORC2/Akt信号通路促进细胞生长
为探究Cas9调控细胞生长的信号机制,研究团队进行了多层次的实验验证。首先通过荧光标记的蛋白合成检测评估了Cas9对mRNA翻译效率的影响。随后通过RNA-seq分析Cas9对DU145细胞转录组的全局影响,采用DESeq2进行差异表达分析,并以错误发现率校正后的P值<0.05和|log2(fold change)|≥1为阈值确定显著差异表达基因。通过GO、KEGG和GSEA分析识别受影响的信号通路。最后通过Western blot检测关键信号蛋白的磷酸化水平,并使用特异性抑制剂验证通路依赖性。
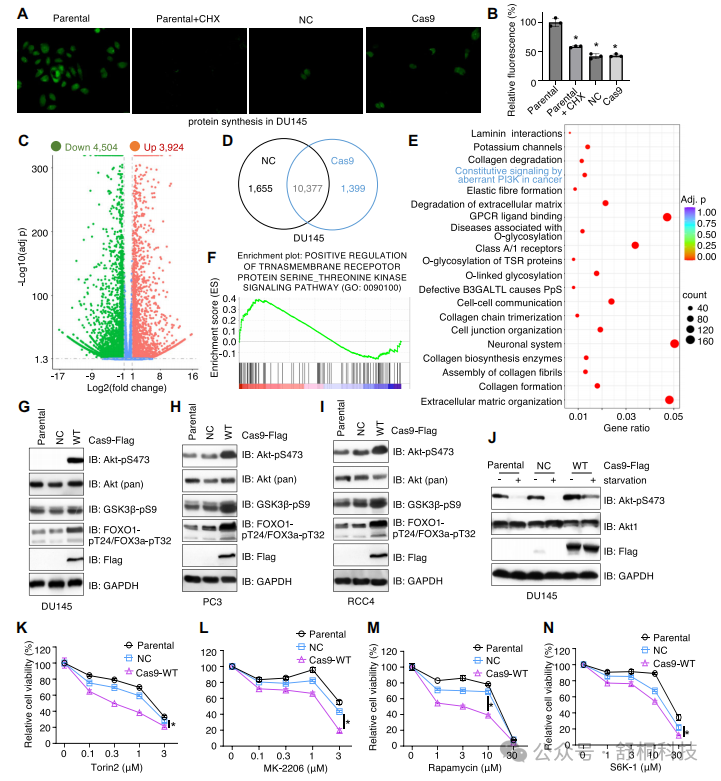
图3 SpCas9通过结合核糖体调控mTORC2激活,对mRNA翻译效率影响微弱
重要实验结论
1. Cas9激活PI3K-Akt-mTOR信号通路:转录组分析显示,Cas9表达显著富集了PI3K-Akt信号通路相关基因,GSEA分析进一步证实了跨膜受体丝氨酸/苏氨酸激酶信号通路的激活(图3C-F)
2. Cas9增强mTORC2激酶活性:在DU145、PC3和RCC4细胞中,Cas9表达显著提高了Akt Ser473位点的磷酸化水平,这是mTORC2的特异性底物(图3G-I)
3. Cas9维持生长因子缺失条件下的mTORC2活性:在血清饥饿条件下,对照细胞中mTORC2活性显著降低,而Cas9表达细胞仍保持较高的Akt磷酸化水平,表明Cas9能绕过生长因子需求激活mTORC2(图3J)
4. Cas9促进的生长依赖于mTORC2/Akt信号:使用Torin 2(mTOR抑制剂)、MK2206(Akt抑制剂)、rapamycin(mTORC1抑制剂)和S6K-I(S6K抑制剂)处理均能显著抑制Cas9表达细胞的生长,证实了该信号通路的关键作用(图3K-N)
Cas9作为分子支架促进核糖体-mTORC2相互作用
为深入解析Cas9激活mTORC2的分子机制,研究团队进行了一系列生化实验。通过免疫共沉淀和GST pull-down实验验证了Cas9、核糖体蛋白和mTORC2组分之间的直接相互作用。通过构建Sin1的不同结构域截短体,鉴定了与核糖体蛋白相互作用的关键区域。利用体外激酶实验评估mTORC2的活性,将免疫沉淀的mTORC2复合物与底物GST-Akt1-tail在含有冷ATP的激酶缓冲液中孵育,通过Western blot检测Akt磷酸化水平。此外,通过siRNA敲低内源核糖体蛋白表达,验证了其在Cas9介导的mTORC2激活中的必要性。
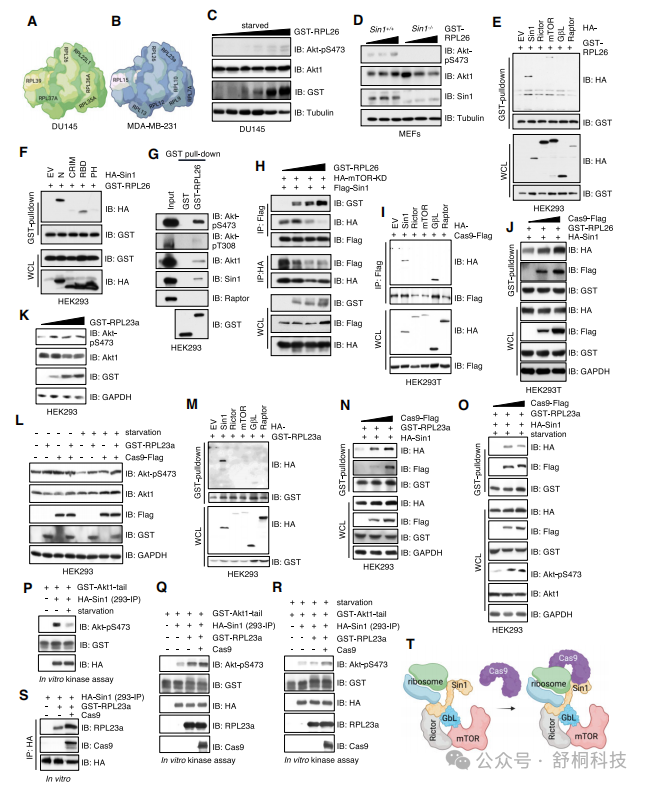
图4 SpCas9增强核糖体与mTORC2的关联以促进mTORC2激活
重要实验结论
1. 核糖体蛋白直接结合mTORC2的Sin1亚基:RPL26和RPL23a能特异性与Sin1结合,而不与其他mTORC2组分相互作用,这种结合主要由Sin1的N端和RBD结构域介导(图4E-G)
2. 核糖体蛋白解除Sin1-PH对mTOR激酶域的抑制:RPL26与Sin1的结合能缓解Sin1-PH结构域对mTOR激酶活性的抑制作用,提供了解释核糖体激活mTORC2的机制(图4H)
3. Cas9直接结合Sin1并增强核糖体-mTORC2相互作用:Cas9通过其PH结构域与Sin1结合,并显著增强RPL26和RPL23a与Sin1的关联,即使在血清饥饿条件下也能维持这种(图4I、J、N、O)
4. Cas9在体外增强mTORC2激酶活性:在无细胞体系中,添加重组Cas9蛋白能增强mTORC2对Akt底物的磷酸化能力,证实了Cas9的直接激活作用(图4Q-R)
研究总结与展望
本研究系统揭示了稳定表达Cas9核酸酶通过调控mTORC2信号通路影响哺乳动物细胞生长的新机制,对CRISPR基因编辑技术的安全应用具有重要启示。研究发现,Cas9作为细菌来源的核酸酶,不仅能执行预期的基因组编辑功能,还能作为支架蛋白增强核糖体与mTORC2信号的相互作用,从而在部分细胞类型中促进细胞生长。这一发现解释了为
什么在不同细胞系中Cas9表达会产生差异性的生长效应,也为理解细菌蛋白与宿主细胞信号网络的相互作用提供了新视角。
研究结果对CRISPR技术的应用提出了重要考量。在基础研究中,特别是基于CRISPR的功能基因筛选中,Cas9稳定表达可能通过改变细胞生长特性而引入偏差,影响筛选结果的解读。在临床应用中,长期表达Cas9的基因治疗策略可能需要评估其对细胞行为的非预期影响,特别是在肿瘤易感个体中的潜在风险。此外,研究还提示,不同细胞类型对Cas9表达的反应存在差异,这在设计基因治疗策略时需予以考虑。
展望未来,基因编辑技术的发展方向应包括:
1. 工程化改造Cas9(如突变与Sin1/RPLs互作界面),开发更安全、细胞干扰更小的变体。
2. 评估其他编辑酶(如Cas12a, Fanzor等)的细胞效应。
3. 在体内模型中进一步验证这些发现。
舒桐科技:助力更安全、高效的基因编辑研究与应用
定制化稳转Cas9解决方案
为应对研究中揭示的Cas9长期表达对细胞生长的影响,舒桐科技提供专业的稳转株构建全流程服务,确保实验模型的可靠性与一致性:
1. 质粒构建:采用优化设计的载体骨架与表达元件,精确调控Cas9表达水平,从源头上规避因过表达引起的细胞毒性
2. 病毒包装:提供高滴度、高感染效率的慢病毒包装服务,确保Cas9基因的高效递送与稳定整合,支持多种难转染细胞系的模型构建
3. 稳转株构建:通过多克隆筛选与单克隆分离技术,结合表达水平验证与功能测试,获得遗传背景一致、编辑活性稳定的细胞株系
优化核酸酶平台
舒桐科技提供多样化的高活性核酸酶(SpCas9, nCas9, dCas9, Cas12a,, PE等),并持续进行工程化改造,旨在开发编辑效率高、脱靶风险低、细胞干扰小的新型酶系统,响应本研究揭示的安全需求:
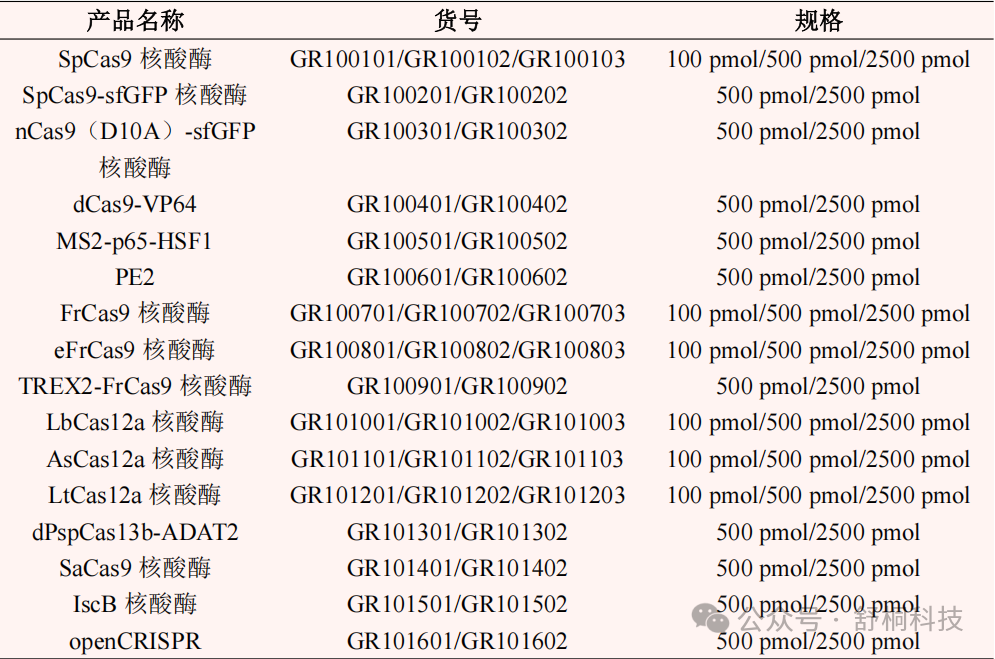
安全评估服务体系
依托对基因编辑技术的深入理解,舒桐科技建立了全面的安全性评估服务:
1. 脱靶效应检测:采用全基因组测序等先进方法,全面评估基因编辑工具的脱靶情况,确保编辑特异性
2. 长期表达安全性:研究核酸酶长期表达对细胞行为的影响,为临床应用提供安全性依据
定制化基因编辑解决方案
针对不同应用场景,舒桐科技提供专业定制服务:
1. 研究用基因编辑工具:为基础研究提供高效、可靠的CRISPR试剂和设计方案,助力基因功能发现
2. 临床前开发支持:为基因治疗开发提供临床前评估、载体设计和安全性测试服务,加速转化进程
3. 特异性应用优化:根据客户特定需求,优化编辑系统效率和特异性,提供最适合的解决方案
随着基因编辑技术的不断发展和完善,舒桐科技将继续秉承“创新、敬业、融合、开放”的理念,与科研界和产业界共同努力,推动基因编辑技术向更安全、更有效的方向发展,为人类健康和生命科学进步贡献力量。通过持续的技术创新和对科学前沿的深入理解,我们相信基因编辑技术将在未来发挥更加重要的作用,为多种难治性疾病的治疗带来新的希望。